關于非法冒用樂研品牌名義傳播不實郵件的聲明
隨著樂研品牌(leyan.com)的影響力和知名度不斷提升,近期遭到不法人員冒用樂研品牌名義,以非法途徑冒用樂研名義,甚至冒充樂研高管,向客戶群發不實‘開學季活動’的郵件,企圖誤導正常的商業合作,此行為嚴重影響樂研品牌形象與聲譽。
在此,樂研品牌聲明如下:
1、樂研正式的郵箱后綴與官網相同,均為@leyan.com,不存在其他形式的郵箱域名;任何其他形式的域名郵件地址,均為不法人員注冊的垃圾郵件。
2、網絡非法外之地,不法分子的惡劣行徑蓄意破壞行業環境,樂研對此行為絕不姑息并將追究法律責任。
3、如各位業務伙伴收到相關郵件或信息,請立即向樂研舉報,聯系電話:400-8210-725
上海皓鴻生物醫藥科技有限公司
2023年4月12日
特此公告!
-
技術服務Service
-
定制合成研發
技術領先,致力于技術壁壘高、合成難度大、附加值高的新穎藥物分子砌塊的研發 -
工藝開發
公斤級的中試實驗室,100+資深研發人員,高效的工藝路線篩選和安全性評估體系 -
檢測方法開發
專業的分析研發和質量控制團隊,為您提供全方位的分析方法開發、驗證和測試服務 -
固態化學 & 單晶研究
晶型/鹽型/共晶篩選、固態分析、結晶工藝研究服務,單晶培養、檢測、解析服務 -
多肽定制合成服務
專業提供2~60肽定制服務,包含線性肽、樹狀支鏈多肽、環肽和多種特殊修飾的多肽 -
GMP工廠生產
樂研提供的GMP相關原料藥和中間體嚴格遵守GMP指南生產,保證化合物的安全、可靠、穩定和高質量 -
寡核苷酸定制服務平臺
專業豐富的化學修飾能力與技術,滿足各種功能的定制需求
-
-
 技術支持
技術支持




 400-821-0725
400-821-0725
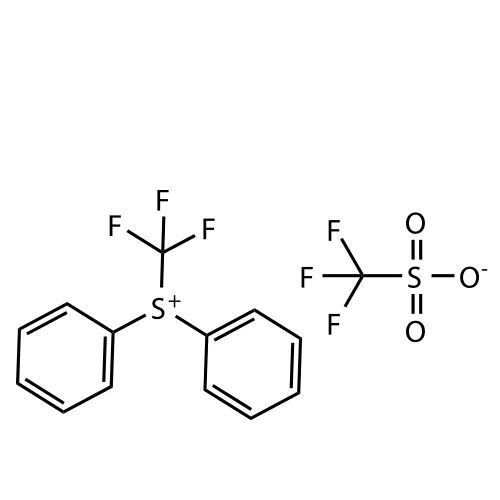
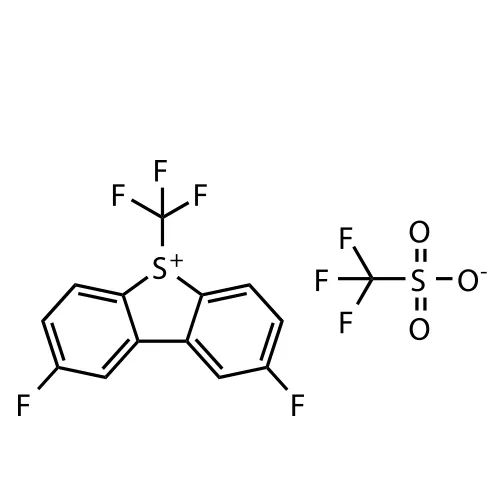
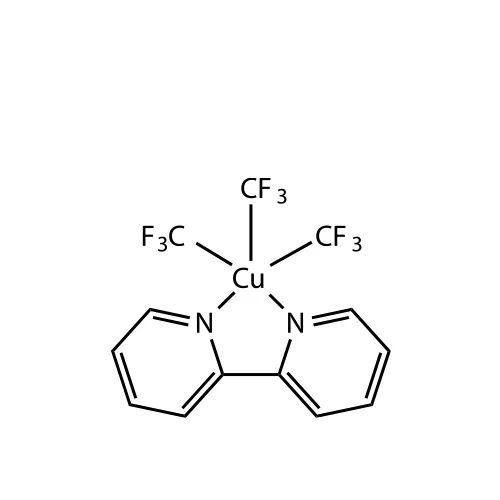
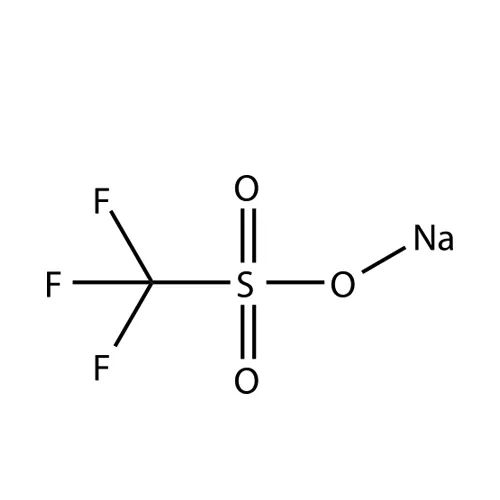


 滬ICP備17019645號
滬ICP備17019645號







